LAWS AND PROPERTIES OF PERFECT GASES
Other Chapters
FUNDAMENTALS OF THERMODYNAMICSLAWS AND PROPERTIES OF PERFECT GASESTHERMODYNAMIC PROCESS AND CYCLESFORMATION AND PROPERTIES OF STEAMSTEAM BOILERS AND PERFORMANCESTEAM AND GAS TURBINEINTERNAL COMBUSTION ENGINESAIR COMPRESSORS AND THEIR PERFORMANCEREFRIGERATION AND AIR CONDITIONING
- س1: مثالی گیس / کامل گیس (Ideal Gas / Perfect Gas) کی تعریف کریں۔جواب: مثالی گیس یا کامل گیس ایک فرضی گیس ہے جو تمام درجہ حرارت اور دباؤ پر تمام گیس قوانین کی سختی سے پیروی کرتی ہے۔ اس گیس میں یہ فرض کیا جاتا ہے کہ مالیکیولز کا حجم نہ ہونے کے برابر ہے اور ان میں کشش یا دفع کی کوئی باہمی قوت نہیں ہے۔
- س2: گیس کی خصوصیتی مساوات (Characteristic Gas Equation) کیا ہے؟جواب: گیس کی خصوصیتی مساوات دباؤ، حجم، اور درجہ حرارت کے درمیان تعلق کو ظاہر کرتی ہے۔ یہ اس طرح بیان کی جاتی ہے:
PV = mRT
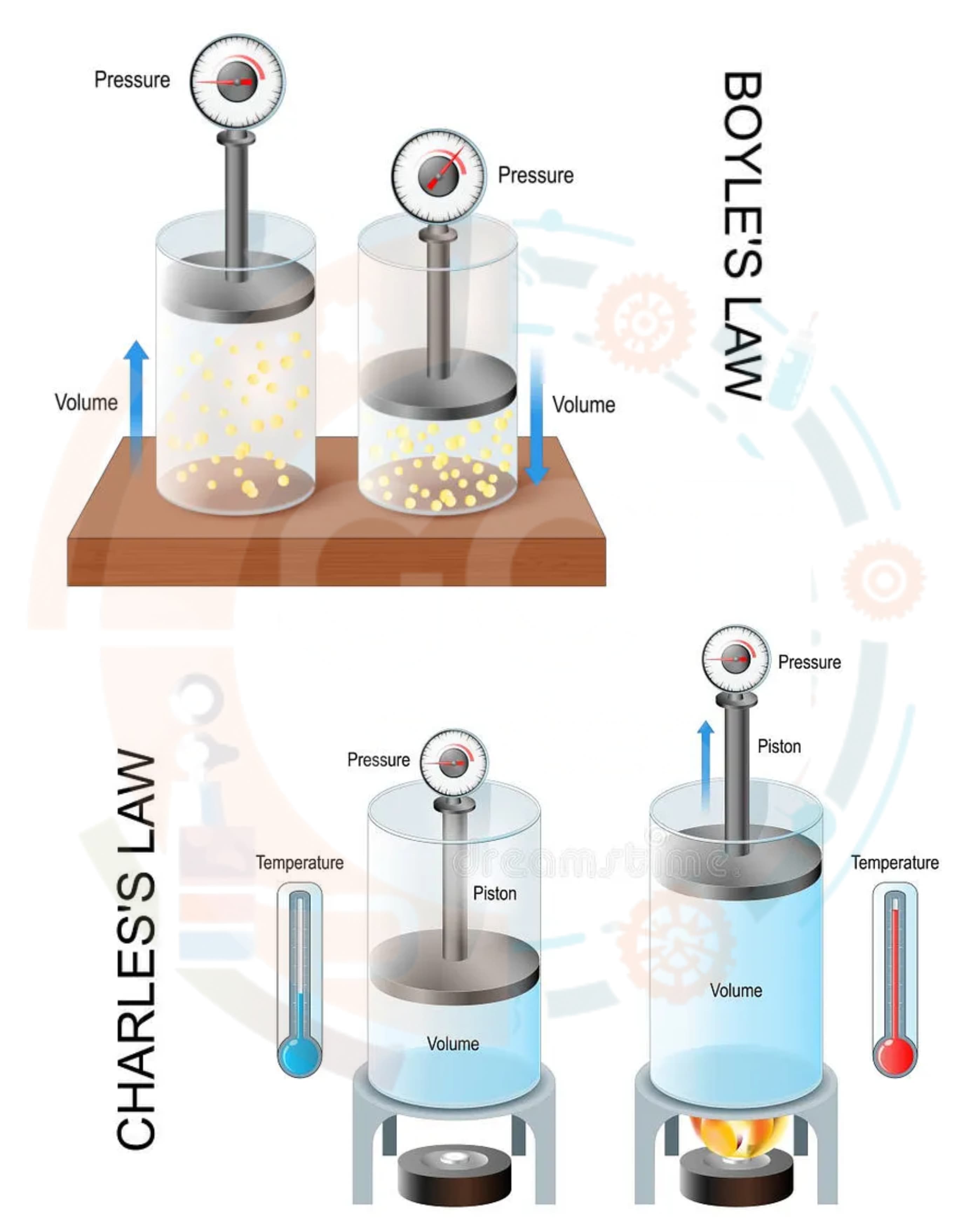
جہاں: P = دباؤ, V = حجم, m = ماس, R = گیس مستقل, T = مطلق درجہ حرارت۔ - س3: بوائل کا قانون (Boyle's Law) کی تعریف کریں۔جواب: بوائل کا قانون کہتا ہے کہ کسی مقررہ ماس کی گیس کے لیے اگر درجہ حرارت مستقل ہو، تو گیس کا دباؤ اس کے حجم کے الٹا متناسب ہوتا ہے۔ اس کا مطلب ہے کہ جب حجم کم ہوتا ہے، تو دباؤ بڑھتا ہے بشرطیکہ درجہ حرارت مستقل رہے۔
مساوات:
PV = مستقل - س4: چارلس کا قانون (Charles’s Law) کی تعریف کریں۔جواب: چارلس کا قانون کہتا ہے کہ کسی مقررہ ماس کی گیس کے لیے اگر دباؤ مستقل ہو، تو گیس کا حجم اس کے مطلق درجہ حرارت کے ساتھ براہ راست متناسب ہوتا ہے۔ اگر درجہ حرارت بڑھتا ہے تو حجم بھی بڑھتا ہے۔
مساوات:
V / T = مستقل - س5: گی-لوساک کا قانون (Gay-Lussac Law) کی تعریف کریں۔جواب: گی-لوساک کا قانون کہتا ہے کہ کسی مقررہ ماس کی گیس کے لیے اگر حجم مستقل ہو، تو گیس کا دباؤ اس کے مطلق درجہ حرارت کے ساتھ براہ راست متناسب ہوتا ہے۔ اس طرح، جب درجہ حرارت بڑھتا ہے، تو دباؤ بھی بڑھتا ہے۔
- س6: جول کا قانون (Joule’s Law) کی تعریف کریں۔جواب: جول کا قانون کہتا ہے کہ مثالی گیس کی داخلی توانائی صرف اس کے درجہ حرارت پر منحصر ہوتی ہے اور دباؤ یا حجم سے آزاد ہوتی ہے۔ اس کا مطلب یہ ہے کہ درجہ حرارت میں تبدیلی داخلی توانائی میں تبدیلی کا سبب بنتی ہے۔
- س7: اوگوادر کا قانون (Avogadro’s Law) کی تعریف کریں۔جواب: اوگوادر کا قانون کہتا ہے کہ تمام گیسوں کے برابر حجم، ایک ہی درجہ حرارت اور دباؤ پر برابر تعداد میں مالیکیولز پر مشتمل ہوتے ہیں۔ لہذا، حجم مولز کی تعداد کے ساتھ براہ راست متناسب ہوتا ہے۔
- س8: ڈالٹن کا قانون (Dalton’s Law) کی تعریف کریں۔جواب: ڈالٹن کا قانون کہتا ہے کہ غیر ردعمل پذیر گیسوں کے مجموعے کا کل دباؤ ہر انفرادی گیس کے جزوی دباؤ کے مجموعے کے برابر ہوتا ہے۔
- س9: ریگنو کا قانون (Regnault’s Law) کی تعریف کریں۔جواب: ریگنو کا قانون کہتا ہے کہ کسی گیس کے لیے مستقل دباؤ پر مخصوص حرارت مستقل حجم پر مخصوص حرارت سے زیادہ ہوتی ہے۔ اس کی وجہ یہ ہے کہ مستقل دباؤ پر کچھ حرارت خارجی کام کرنے میں استعمال ہوتی ہے۔
- س10: عمومی گیس مساوات (General Gas Equation) کیا ہے؟جواب: عمومی گیس مساوات بوائل کا قانون، چارلس کا قانون، اور گی-لوساک کے قانون کو ملا کر بیان کی جاتی ہے۔ کسی مقررہ ماس کی گیس کے لیے یہ یوں لکھی جاتی ہے:
P1V1 / T1 = P2V2 / T2 - س11: عالمی گیس مساوات (Universal Gas Equation) کیا ہے؟جواب: عالمی گیس مساوات دباؤ، حجم، اور درجہ حرارت کو گیس کے مولز کے لحاظ سے بیان کرتی ہے۔ یہ یوں لکھی جاتی ہے:
PV = nRuT
جہاں n = مولز کی تعداد، اور Ru = عالمی گیس مستقل۔ - س12: خصوصی حرارت (Specific Heat) کی تعریف کریں۔جواب: خصوصی حرارت وہ مقدار حرارت ہے جو کسی مادے کے ایک کلوگرام کے درجہ حرارت کو ایک سیلسیس یا ایک کیلون سے بڑھانے کے لیے درکار ہوتی ہے۔ یہ مادے کی حرارت ذخیرہ کرنے کی صلاحیت کو ظاہر کرتی ہے۔
- س13: گیس کی دو خصوصی حرارتیں بتائیں۔جواب: گیس کی دو خصوصی حرارتیں یہ ہیں:
- ● مستقل حجم پر خصوصی حرارت (Cv)
- ● مستقل دباؤ پر خصوصی حرارت (Cp)
- س14: مولر خصوصی حرارت (Molar Specific Heat) کی تعریف کریں۔جواب: مولر خصوصی حرارت وہ مقدار حرارت ہے جو کسی مادے کے ایک مول کے درجہ حرارت کو ایک کیلون بڑھانے کے لیے درکار ہوتی ہے۔ اسے حرارت فی مول فی ڈگری درجہ حرارت کے حساب سے بیان کیا جاتا ہے۔
- س15: گیس کی اینٹروپی (Entropy) کی تعریف کریں۔جواب: گیس کی اینٹروپی وہ خاصیت ہے جو ظاہر کرتی ہے کہ گیس میں توانائی کس حد تک منتشر یا بےترتیب ہے۔ جب مالیکیولز زیادہ بےترتیب حرکت کرتے ہیں اور توانائی کم دستیاب ہوتی ہے مفید کام کے لیے، تو اینٹروپی بڑھ جاتی ہے۔
- س16: گیس کی اینتھالپی (Enthalpy) کی تعریف کریں۔جواب: گیس کی اینتھالپی گیس کی کل حرارت کی مقدار ہے۔ یہ داخلی توانائی اور دباؤ اور حجم کے حاصل ضرب کا مجموعہ ہے، جسے یوں لکھا جاتا ہے: H = U + PV۔
- س17: کارنوٹ سائیکل (Carnot Cycle) کیا ہے؟جواب: کارنوٹ سائیکل ایک مثالی تھرموڈائنامک سائیکل ہے جو دو مساوی حرارت والے (isothermal) عمل اور دو adiabatic عمل پر مشتمل ہوتا ہے۔ یہ دو درجہ حرارت کی حدود کے درمیان سب سے مؤثر حرارت انجن سائیکل کی نمائندگی کرتا ہے۔
- س18: گیس مستقل (Gas Constant) کی قیمت کیا ہے؟جواب: ہوا کے لیے گیس مستقل کی قیمت R = 287 J/kgK ہے۔
- س19: عالمی گیس مستقل (Universal Gas Constant) کی قیمت کیا ہے؟جواب: عالمی گیس مستقل کی قیمت R = 8314 J/kgK ہے۔